EMA a aprobat luni administrarea celei de-a treia doze de vaccin Pfizer/BioNTech la persoanele peste 18 ani
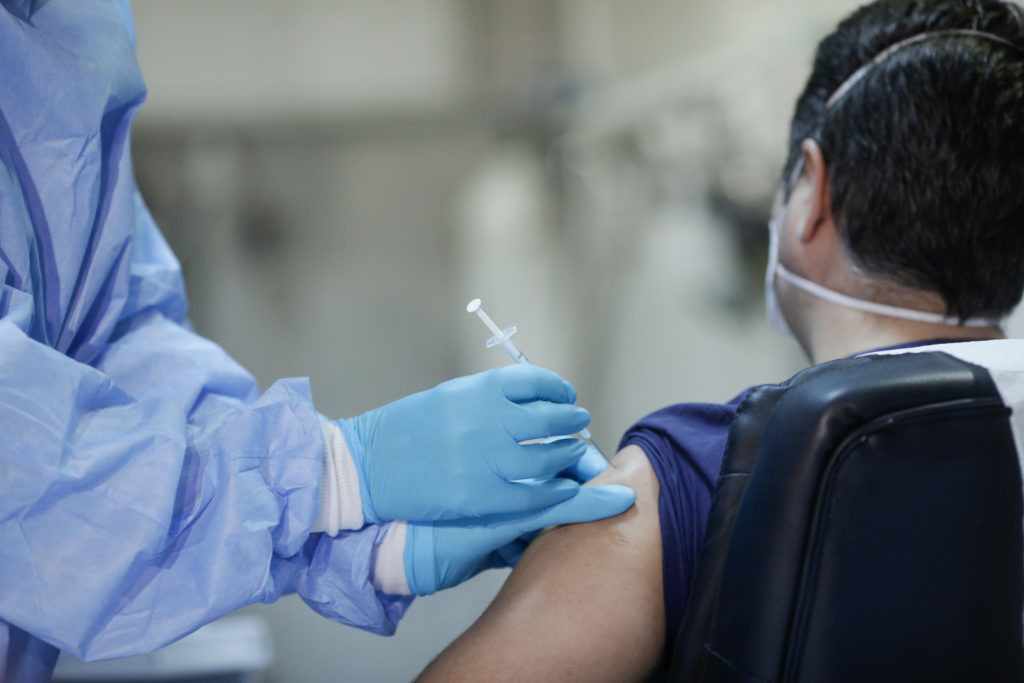
Agenţia Europeană a Medicamentului (EMA) a aprobat luni administrarea celei de-a treia doze de vaccin Pfizer/BioNTech la persoanele peste 18 ani, precizând că protecţia împotriva COVID-19 ar putea să scadă după primele două doze, relatează AFP.
„Dozele de rapel de Comirnaty (Pfizer/BioNTech) pot fi luate în considerare pentru persoanele cu vârsta de 18 ani şi peste, la cel puţin şase luni de la a doua doză”, a indicat EMA într-un comunicat, referindu-se la denumirea comercială a vaccinului Pfizer.
Doze suplimentare de vaccinuri Moderna şi Pfizer pentru persoanele cu sistem imunitar foarte slăbit au fost, de asemenea, aprobate de Agenţia Europeană a Medicamentului, cu sediul la Amsterdam.
„Deciziile privind a treia doză vor fi luate de organismele de sănătate publică la nivel naţional”, a precizat EMA.
Comitetul EMA pentru medicamente de uz uman (CHMP) a „evaluat datele pentru Comirnaty care indică niveluri crescute de anticorpi la administrarea unei a treia doze”.
„Nu se cunoaşte riscul apariţiei de boli cardiace inflamatorii sau a altor reacţii adverse foarte rare după un rapel şi acest aspect este atent monitorizat”, a adăugat EMA.
Cazuri rare de miocardită, o inflamaţie a muşchiului inimii, au fost raportate la persoanele care au primit vaccinul Pfizer, în special la bărbaţii tineri.
Totodată, EMA a dat undă verde persoanelor cu un „sistem imunitar foarte slăbit” pentru a fi vaccinate cu doze suplimentare de Moderna şi Pfizer, la cel puţin 28 de zile de la a doua doză.
Două doze de vaccin nu sunt suficiente uneori pentru a produce suficienţi anticorpi la persoanele imunocompromise, precum cele care au suferit un transplant de organe.
„Deşi nu există dovezi directe conform cărora capacitatea de a produce anticorpi la aceşti pacienţi îi protejează împotriva COVID-19, este de aşteptat că doza suplimentară să crească protecţia cel puţin la unii pacienţi”, a afirmat EMA. AGERPRES